El Mes de los Primates Neotropicales y una misión compartida
Ariel Rodríguez-Vargas
Marzo es el mes de los primates, que no es una fiesta. Marzo es un recordatorio de trabajo por hacer para garantizar su protección en todos nuestros países latinoamericanos. Una llamada de atención que nos interpela desde las copas de los árboles, desde los fragmentos de bosque que aún resisten, desde los corredores biológicos que necesitamos construir con urgencia. El mes de los primates neotropicales no se celebra, se reflexiona. Se conmemora con acciones concretas, con cuadernos en las escuelas, con cámaras trampa en el campo, con decretos municipales, con nuevas áreas protegidas y con conversaciones incómodas en las ciudades. Lo que está en juego no es un desfile de especies carismáticas. Lo que está en juego es la integridad ecológica de todo un continente. Y protegerla requiere que todos, absolutamente todos, nos involucremos de manera activa y consciente.
Lo que está en juego no es un desfile de especies carismáticas. Lo que está en juego es la integridad ecológica de todo un continente. Y protegerla requiere que todos, absolutamente todos, nos involucremos de manera activa y consciente.
Territorio
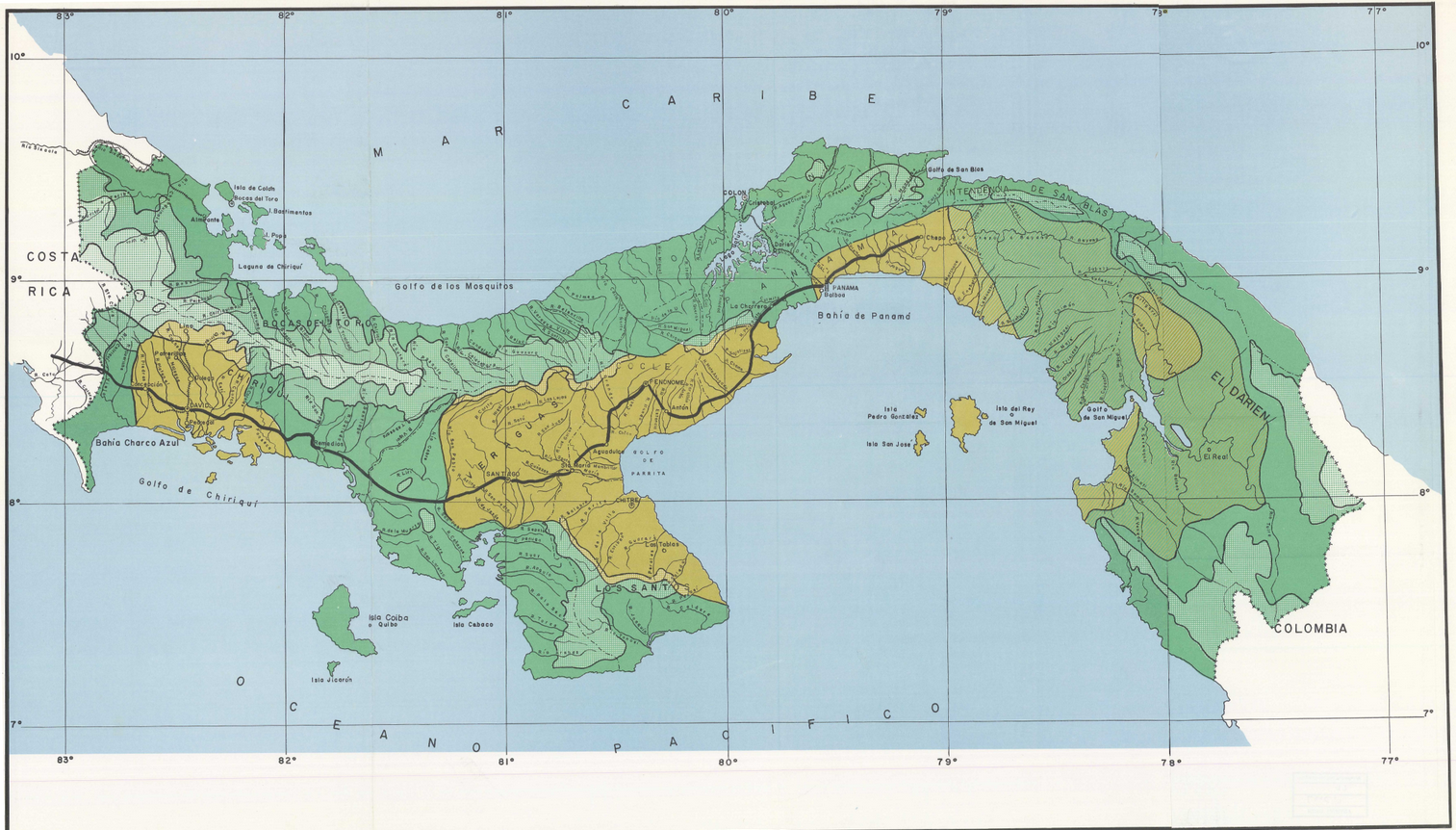
Somos América Latina, la región más biodiversa del continente, la tierra de los primates neotropicales. Una región que se extiende desde Veracruz en el Caribe mexicano hasta los bosques subtropicales de Argentina, pasando por el istmo centroamericano, la inmensidad del Amazonas, los Andes y el Bosque Atlántico.
Somos Latinoamérica, el hogar de una de las radiaciones evolutivas más espectaculares del planeta. Los platirrinos, o primates del Nuevo Mundo, representan con más de 200 especies un tercio de todos los primates del mundo. Somos los guardianes de una diversidad biológica sin igual. Desde el tití pigmeo, Cebuella pygmaea, que con sus 100 gramos cabe en la palma de una mano, hasta el majestuoso muriquí, Brachyteles, que puede pesar 15 kilos y es el primate más grande de América, cada especie es una solución única a los desafíos de la vida en los árboles y al complejo ecosistémico de bosque tropical.
Imaginemos un mapa de nuestros países donde somos la América tropical y dibujemos sobre él las grandes cuencas hidrográficas. El río Amazonas, con sus afluentes, no es solo una red de agua. Es la autopista que ha moldeado la evolución de los primates durante milenios. Cada gran río, el Madeira, el Tapajós, el Negro, el Orinoco, actúa como una barrera natural que ha permitido que especies hermanas sigan caminos evolutivos distintos, creando la asombrosa diversidad que vemos hoy.
Al norte, en México, Guatemala y Belice, los monos aulladores, Alouatta pigra y A. palliata, y los monos araña, Ateles geoffroyi, nos recuerdan que la influencia de los primates llega hasta más allá de los confines del mundo maya. En Centroamérica, desde Honduras hasta Panamá, se suma el capuchino de cara blanca, Cebus imitator, ese curioso explorador que tanto nos hace reflexionar con su inteligencia. En Panamá ya encontramos además el capuchino panameño, el mono nocturno y el tití panameño (Saguinus). En una pequeña zona de Chiriquí y la zona sur y central de Costa Rica, aparece el mono tití chiricano o mono ardilla (Saimiri oerstedii), una especie amazónica que evolucionó en Centroamérica!
Bajamos desde Mesoamérica hacia Colombia y Venezuela, y la diversidad explota. Aquí encontramos especies endémicas como el mono araña de Magdalena, Ateles hybridus, y el tití cabeciblanco, Saguinus oedipus, joyas de la biodiversidad que no existen en ningún otro lugar del mundo.
El Ecuador y Perú son el corazón de la diversidad de primates del gran subcontinente llamado Sudamérica. En sus selvas amazónicas y bosques nublados conviven más de 30 especies, desde los diminutos titís pigmeos hasta los imponentes monos lanudos. Y qué decir de Bolivia, con sus bosques secos chaqueños donde el mono aullador negro y dorado, Alouatta caraya, demuestra que los primates también saben prosperar fuera de la selva húmeda.
Brasil, el país gigante, alberga la mayor diversidad, con endemismos únicos como los muriquís del Bosque Atlántico y los uakarís de la Amazonía central. Paraguay y el norte de Argentina son la frontera sur de esta gran historia, donde los mirikinás, Aotus azarae, desafían el frío chaqueño con una flexibilidad conductual asombrosa.
La diversidad de primates neotropicales nos llevan a ser testigos del extremo las soluciones evolutivas que han logrado. Porque en sus adaptaciones está la clave para entender cómo configuran el bosque, con los hábitats claves para su supervivencia. En todo esta enorme región tenemos primates grandes y diminutos, amistosos, enigmáticos e inteligentes, y todos tienen una particularidad que nos debe inspirar a ser responsables de su cuidado.
El gigante amistoso
El muriquí del norte, Brachyteles hypoxanthus, es el primate más grande de América. Un macho adulto puede superar los 15 kilogramos y, cuando extiende sus largos brazos, parece abrazar el mundo. Pero lo extraordinario de este gigante no es su tamaño, sino su personalidad. En los grupos de muriquís no existen las jerarquías de dominancia. Los conflictos se resuelven con abrazos, no con peleas. Las hembras eligen libremente a sus parejas y los machos cooperan entre sí como si hubieran descubierto, antes que nosotros, que la violencia es un callejón sin salida.
Viven exclusivamente en los fragmentos de Bosque Atlántico del sureste brasileño, y su presencia es un termómetro de salud ecológica. Donde hay muriquís, hay bosque maduro con árboles gigantes capaces de sostener a estos pacifistas que necesitan cientos de hectáreas para vivir.
El pequeño pigmeo
En el extremo opuesto de la balanza, el tití pigmeo, Cebuella pygmaea, cabe en la palma de una mano. Con sus 100 gramos de peso, es el primate más pequeño del mundo. Pero su tamaño reducido no es una limitación. Es una estrategia maestra. Su pequeñez le permite acceder a las ramas más delgadas del dosel, donde otros primates no pueden llegar. Y sus incisivos, afilados como cinceles, le permiten hacer algo único. Perforar la corteza de los árboles para lamer la goma que fluye.
Este recurso, los exudados vegetales, está disponible todo el año, lo que libera al tití pigmeo de depender de frutos estacionales. Vive en grupos familiares donde todos ayudan a criar a los gemelos, y sus llamados ultrasónicos, inaudibles para muchos depredadores, les permiten coordinarse sin ser detectados.
El Enigmático
Si hay un primate que merece el título de enigma viviente, ese es el mico de Goeldi, Callimico goeldii. Durante décadas, los científicos no sabían dónde ubicarlo en el árbol genealógico. Tiene garras como los titís, pero 36 dientes como los monos cébidos más grandes. Vive en los bosques de bambú del suroeste amazónico, en poblaciones tan fragmentadas y discretas que parece un fantasma.
Pero su rareza más fascinante es dietética pues es el único primate neotropical que consume hongos de manera habitual. Hasta el 40% de su dieta en la estación húmeda puede ser setas, un recurso que nadie más aprovecha. Y a diferencia de todos sus parientes calitrícidos, que casi siempre tienen gemelos, el mico de Goeldi tiene una sola cría por parto. Es como si la evolución hubiera dicho que va a probar algo completamente diferente.
El Inteligente de los bosques
Los capuchinos robustos del género Sapajus son los dueños del coeficiente intelectual del bosque. Su cerebro es tan grande en proporción a su cuerpo como el de un chimpancé. Pero no es solo tamaño. Es lo que hacen con él.
En las sabanas arboladas del noreste de Brasil, los capuchinos de barba, Sapajus libidinosus, seleccionan piedras de distintos tamaños y pesos, las transportan hasta yunques naturales y las usan para romper nueces de palma. No es un comportamiento instintivo. Es una tradición cultural que las madres enseñan a sus crías durante años de aprendizaje. Un joven capuchino puede tardar hasta ocho años en dominar la técnica, observando, imitando y practicando.
Pero además de usar herramientas, los capuchinos cazan cooperativamente, se reconocen en espejos, planean rutas de forrajeo y resuelven problemas novedosos con una creatividad que asombra a los científicos. Son los filósofos del dosel.
El adaptado vegetariano
Si hay un primate que ha conquistado todos los rincones del Neotrópico, ese es el mono aullador, Alouatta. Desde el sur de México hasta el norte de Argentina, desde las selvas húmedas hasta los bosques secos del Chaco, los aulladores están presentes donde ningún otro primate se atreve.
Su secreto es la hoja. Mientras otros monos compiten por frutos escasos, los aulladores desarrollaron un estómago complejo, dividido en cámaras, donde bacterias especializadas fermentan las hojas y extraen nutrientes. Es una dieta disponible todo el año. Su recompensa es poder vivir con un metabolismo lento que les permite pasar hasta el 70% del día descansando. Y en los adultos machos su herramienta de comunicación es un hueso hioides agrandado que actúa como caja de resonancia, que les permite producir aullidos que pueden llegar varios kilómetros de distancia, demarcando territorios sin gastar energía en peleas. Las hembras y juveniles también emites sonidos peculiares.
El mono araña del bioma del Chocó
El mono araña negro, Ateles fusciceps, confinado a los bosques del bioma del Chocó en Panamá, Colombia y Ecuador, tiene una población pequeña de individuos maduros. El tití león de cara negra, Leontopithecus caissara, endémico de una pequeña franja costera en el sur de Brasil, no supera los 400 individuos. El mono lanudo de cola amarilla, Lagothrix flavicauda, en los bosques nublados del norte de Perú, ha perdido más del 80% de su hábitat.
Estos números no son fríos. Detrás de cada cifra hay grupos sociales que se desintegran, tradiciones culturales que se pierden, linajes evolutivos de 40 millones de años que se apagan para siempre.
Nichos ecológicos de los primates neotropicales
Lo más fascinante de los primates neotropicales no es solo dónde viven, sino cómo viven y los roles ecológicos que desempeñan. Han aprendido a ocupar absolutamente todos los nichos que el bosque ofrece, como comensales en un banquete interminable donde cada quien tiene su plato favorito.
Los frugívoros o comensales de frutos estrictos son como los jardineros del dosel. Los monos araña, Ateles, y los monos lanudos, Lagothrix, son los conocedores de frutas. Su dieta se compone en un 80 a 90% de frutos maduros. Han desarrollado una memoria espacial prodigiosa para recordar dónde y cuándo fructifica cada árbol a lo largo del año. Son esparcidores de semillas del bosque, porque al tragar las semillas y desplazarse largas distancias, las siembran con abono incluido. Sin ellos, los bosques perderían gran parte de su capacidad de regenerarse con árboles de madera dura y frutos grandes.
Los folívoros son los meditadores del dosel. Los monos aulladores, Alouatta, tomaron un camino distinto. ¿Para qué competir por frutos escasos si las hojas están disponibles todo el año? Su recompensa es poder vivir con una dieta de baja calidad, pero su costo es un metabolismo lento que los obliga a pasar hasta el 70% del día descansando.
Los insectívoros-frugívoros son los energéticos del grupo. Los monos ardilla, Saimiri, tienen un metabolismo acelerado que los obliga a alimentarse casi constantemente. Son pequeños, nerviosos, y viven en tropas enormes de hasta 300 individuos en la amazonía, pero los de Centroamérica son grupos entre 25 y 70 miembros. Su dieta combina insectos con frutos pequeños, y su hiperactividad es una estrategia para maximizar el encuentro con presas y mantener la vigilancia colectiva contra depredadores.
Los exudativoros son los carpinteros en miniatura. Los titís pigmeos y sus primos, los titís del género Mico y Callithrix, han desarrollado incisivos en forma de cincel para acceder a las gomas de los árboles, un recurso energético disponible todo el año.
Los granívoros son los rompedores de nueces. Los capuchinos robustos, Sapajus, del Cerrado y la Caatinga brasileña son los únicos primates americanos que fabrican herramientas de manera habitual, usando piedras como martillos y yunques. En Panamá se ha registrado en cámaras el uso cotidiano de herramientas por parte de Cebus imitator y también se les ha visto robar bebés de monos aulladores para tenerlos de mascota, un acto muy avanzado en la escala evolutiva de estos monos.
Los depredadores de semillas son los especialistas extremos. Los sakis, Pithecia, los Chiropotes, y los uakarís, Cacajao, poseen incisivos procumbentes que les permiten romper frutos con cáscaras leñosas para extraer las semillas.
Los nocturnos son los misteriosos cuando cae la noche. Los micos nocturnos o jujunás, Aotus, son los únicos primates verdaderamente nocturnos del mundo. Con sus enormes ojos adaptados a la penumbra, dominan un turno que nadie más quiere. Este nicho basado en el día y la noche sería como un nicho ligada a sus horas de actividad.
Funciones de los primates neotropicales
Detrás de estos récords o datos importantes hay una función ecológica irreemplazable. Los primates no son meros habitantes del bosque. Son sus ingenieros de tiempo completo.
Los monos araña y los monos lanudos, frugívoros estrictos, son los jardineros del dosel. Al tragar semillas grandes y desplazarse largas distancias, las siembran con abono incluido lejos del árbol padre. Los árboles de madera dura y frutos grandes dependen casi exclusivamente de ellos para regenerarse. Sin monos araña, el bosque se vuelve más homogéneo, dominado por especies de semillas pequeñas dispersadas por el viento.
Los aulladores, al consumir hojas, regulan el crecimiento de las plantas y reciclan nutrientes a través de sus heces. Los capuchinos, al romper nueces y ramas en busca de insectos, crean microhábitats donde otras especies encuentran refugio. Los titís pigmeos, al perforar cortezas, estimulan la producción de gomas que luego aprovechan otras aves y mamíferos.
Los primates son los conectores de la red trófica. Son el alimento de jaguares, pumas, águilas harpías y boas. Donde desaparecen los monos, los depredadores pierden su fuente principal de proteína y se ven forzados a acercarse a zonas humanas en busca de ganado, aumentando el conflicto.
Responsabilidad
Frente a la destrucción del hábitat y otros factores que operan contra las poblaciones de primates neotropicales, todos tenemos un papel. No se trata de esperar a que los gobiernos o las grandes oenegés hagan algo. Se trata de entender que la conservación empieza donde cada uno está parado.
¿Qué hacer desde la ciencia?
La responsabilidad no termina en publicar artículos científicos en revistas. Entre las tareas del científico hay un listado extenso de tareas que van desde el traducir el conocimiento, o sea, los datos sobre la densidad poblacional, genética o ecología del comportamiento son inútiles si no los convertimos en herramientas para quienes toman decisiones en el terreno. Debemos producir mapas de prioridades, guías de identificación para guardaparques, protocolos de monitoreo comunitario. También se deben formar capacidades locales, donde el conocimiento debe quedarse en los territorios. Capacitar a técnicos, guías y estudiantes locales asegura que la investigación tenga continuidad más allá de nuestros proyectos.
Igualmente es responsabilidad escuchar el conocimiento tradicional. Las comunidades que han vivido generaciones en el bosque saben cosas que nosotros tardaríamos décadas en descubrir. Integrar su saber con el nuestro no es solo ético. Es inteligente.
No menos importante es también ser voceros. Tenemos el privilegio de entender la complejidad de estos sistemas. Eso viene con la responsabilidad de hablar en público, escribir para audiencias no especializadas, aparecer en medios. No podemos encerrarnos en la torre de marfil de la academia, como si fuéramos los reyes del conocimiento pero desconectados de la sociedad y de ajenos a la urgencia de acciones.
Cómo involucrar a la sociedad desde la ciudad
La gente en las ciudades no ve monos todos los días, pero sus decisiones afectan directamente el destino de los primates.
Urge la comprensión sobre el consumo responsable. Aprender, por ejemplo, que la soja que alimenta los pollos que comemos, la palma aceitera en los procesados, la madera de los muebles, la carne de res que llega a la mesa, todo tiene una huella en el mapa de deforestación y de destrucción significativa de la biodiversidad. Elegir productos con certificaciones sostenibles no es un acto de hipocresía. Es votar con el bolsillo por el tipo de mundo que queremos.
Promover un turismo consciente, para cuando viajemos a áreas con primates, busquemos operadores responsables que respeten los códigos de conducta del turismo sostenible y realmente ecológico. Nuestro peso como consumidores puede inclinar la balanza hacia modelos económicos que valoren el bosque en pie.
Exigir transparencia en la gestión de la conservación de los bosques y las áreas protegidas, ya que como ciudadanos, podemos preguntar a nuestros representantes cómo se está invirtiendo el presupuesto, qué se está haciendo para controlar el tráfico de fauna, por qué se siguen aprobando proyectos de infraestructura sin evaluar su impacto en la biodiversidad.
Educar en casa donde entremos en contacto real con los hijos, sobrinos, vecinos sobre la existencia de estos animales, sobre su importancia, sobre las historias fascinantes que hay detrás de cada especie. El primer paso para proteger algo es conocerlo.
Cómo debemos trabajar con las comunidades locales
Las personas que conviven con primates todos los días son los verdaderos guardianes del territorio. Sin su participación activa, cualquier estrategia de conservación está condenada al fracaso.
Reconocer derechos. Los territorios indígenas y comunitarios son, en muchos casos, los que mejor conservan los bosques. Apoyar la autonomía de estas comunidades no es solo una cuestión de justicia social. Es una de las estrategias de conservación más efectivas que existen.
Construir alternativas económicas para el indígena o el campesino que convive de cerca con la vida silvestre. No podemos pedirle a un campesino que deje de cazar si la carne de monte es su única fuente de proteína. Se requiere trabajar con ellos para desarrollar opciones, piscicultura, aves de corral, sistemas agroforestales que combinen cultivos con conservación, turismo comunitario bien manejado.
Valorar el conocimiento local y hacer alianzas de conservación con los cazadores tradicionales que saben dónde están los dormideros, las rutas de paso, los árboles frutales clave que consume la vida silvestre. Ese conocimiento es invaluable para la investigación y el monitoreo. Integrarlo en los proyectos no solo mejora la ciencia, sino que dignifica a quienes lo poseen.
Diseñar juntos las soluciones con inventiva propia y efectiva. Los proyectos de conservación deben diseñarse en mesas donde las comunidades tengan voz y voto, donde sus prioridades, acceso a agua, educación, salud, se integren con los objetivos de conservación. No puede haber conservación sin desarrollo sostenible.
Estrategia
El mes de los primates neotropicales es una oportunidad para sembrar conciencia que debe germinar durante todo el año. Esto implica varias rutas de trabajo comenzando con llevar el tema de los primates a las aulas, a los gremios, a las comunidades y al público en general. No como una unidad más en el libro de ciencias naturales, sino como un hilo conductor para entender ecosistemas, cadenas tróficas, cambio climático y ciudadanía ambiental. Un niño que aprende sobre el tití pigmeo no solo memoriza un dato curioso. Aprende que hay animales tan especializados que dependen de un solo tipo de árbol para sobrevivir, y que si ese árbol desaparece, ellos también.
En la educación básica o primaria, los niños pueden aprender sobre las familias de primates como aprenden sobre sus propias familias. ¿Quién es la mamá? ¿Quién carga a los bebés? ¿Cómo se comunican? ¿Qué comen? A través del juego y el dibujo, pueden interiorizar que los monos tienen vidas sociales complejas, no muy diferentes a las nuestras. Eso los hace seres a los que se les puede tener buena empatía.
En la escuela secundaria, los estudiantes pueden analizar mapas de distribución, calcular áreas de fragmentos de bosque usando imágenes de satélite, debatir sobre los pros y contras de proyectos de infraestructura en términos de conectividad ecológica. Pueden hacer sus propias campañas escolares contra el tráfico de mascotas, involucrando a sus familias y vecinos.
En zonas rurales, donde los niños conviven con primates a diario, la escuela puede ser el espacio para reconciliar el conocimiento tradicional con el científico. Un abuelo que ha vivido toda su vida en el bosque sabe cuándo maduran los frutos que comen los monos, dónde duermen, qué depredadores los acechan. Ese saber puede ser tan valioso como cualquier artículo académico, y merece ser escuchado y valorado.
Llevarlos a los medios
No solo en la sección de naturaleza los domingos, sino en las noticias de política ambiental, en los editoriales sobre ordenamiento territorial, en los programas de variedades donde una celebridad local habla de su encuentro con un mono aullador en su finca. Normalizar la presencia de los primates en la conversación pública es el primer paso para que la gente los vea como parte de su realidad cotidiana, no como una postal exótica. No dejar de pasar un mes sin hacer escritos y artículos divulgativos, formativos y educativos.
Campañas en redes y medios
Historias, no datos. A la gente le mueven las historias, no las estadísticas. La historia de una familia de titís león que sobrevive en un fragmento de Bosque Atlántico gracias a un corredor reforestado por una comunidad. La historia de un mono aullador que cruzó un puente de dosel filmado por una cámara trampa. La historia de un niño que convenció a sus padres de no tener un mono como mascota. Ello lleva a aliados inesperados. Necesitamos que los comunicadores, los artistas, los deportistas, los influenciadores se sumen a la causa. Una publicación de un futbolista famoso sobre la importancia de los primates puede llegar a millones de personas que nunca leerían un artículo científico. Pero tiene que ser genuino, informado, constante.
Hay que construir un contenido útil. Diseñar o publicar mapas que la gente pueda usar para saber si su municipio tiene áreas prioritarias de conservación. Deben hacerse guías para identificar especies y saber qué hacer si encuentran un primate herido o en cautiverio. Directorios de autoridades ambientales y organizaciones a las que reportar casos de tráfico. La información tiene que traducirse en acción.
Infraestructura y áreas protegidas para protegerlos
Necesitamos más corredores biológicos funcionales, pero no basta con decretar un corredor en el papel. Hay que restaurarlo con especies nativas que provean alimento y conectividad. Hay que negociar con propietarios privados, ofrecer incentivos, monitorear su efectividad con cámaras trampa y estudios genéticos que confirmen el flujo de individuos entre fragmentos.
Hay que construir pasos aéreos y puentes monos para protegerlos de las carreteras que atraviesan bosques, los monos araña y los aulladores necesitan estructuras que les permitan cruzar sin riesgo de electrocución o atropello. Muchos países ya tienen experiencias exitosas que debemos replicar en toda la región.
Es necesario seguir creando más áreas protegidas, pero bien manejadas. No sirve de nada tener un parque nacional en el papel si no tiene guardaparques, si no hay control de la caza, si los límites no están señalizados. La infraestructura de conservación incluye puestos de control, sistemas de monitoreo, equipos para brigadas contra incendios, programas de educación ambiental en las comunidades de la zona de amortiguamiento.
Crear centros de rescate y rehabilitación en cada región que lo demande. Para las víctimas del tráfico, esas miles de crías arrancadas de sus madres cada año en toda Latinoamérica, necesitamos espacios dignos donde puedan recuperarse y, cuando sea posible, ser reintroducidas. Pero sobre todo, necesitamos que esos centros no sean el destino final, sino un recordatorio de que la lucha principal es contra el tráfico mismo.
Compromiso
Al recorrer este mosaico de información mezclada con temas de conservación y las adaptaciones de los primates, uno no puede sino sentir asombro. Asombro de que en un solo continente, nuestro continente, hayan evolucionado tantas soluciones distintas a los mismos problemas. Asombro de que estos animales, con los que compartimos más del 90% de nuestro ADN, hayan encontrado formas tan diversas de ser primates. Pero también asombro de que, a pesar de todas las presiones, la vida continúe. Los aulladores mexicanos aún despiertan el amanecer en la Península de Yucatán. Los capuchinos aún rompen nueces en el Cerrado brasileño. Los titís pigmeos aún perforan cortezas en la Amazonía peruana. Los muriquís aún se abrazan en los fragmentos del Bosque Atlántico. Los titíes de Chiriquí, llegan al bosque costero para buscar frutas.
La república de los monos sigue en pie. Pero sus ciudadanos necesitan que nosotros, científicos, urbanistas, campesinos, indígenas, políticos, maestros, periodistas, estudiantes, decidamos, cada uno desde donde está, que queremos seguir siendo sus vecinos, sus guardianes, sus cómplices.
Porque cuando un mono araña cruza un claro del bosque con la gracia de un acróbata, cuando un aullador hace retumbar la selva con su canto, cuando un tití pigmeo se asoma desde una rama con sus enormes ojos, no solo están viviendo sus vidas. Están recordándonos que la biodiversidad no es un lujo ni un adorno. Es en realidad la red que nos sostiene a todos. Si ellos desaparecen, más temprano que tarde seguiremos nosotros.
Y mientras esa red siga vibrante, mientras sigamos tejiéndola con corredores, con escuelas, con leyes, con conciencia, la gran historia de los primates americanos no tendrá razón para terminar.
Este marzo, no celebremos. Actuemos. Y que la acción no termine cuando el calendario cambie de página.
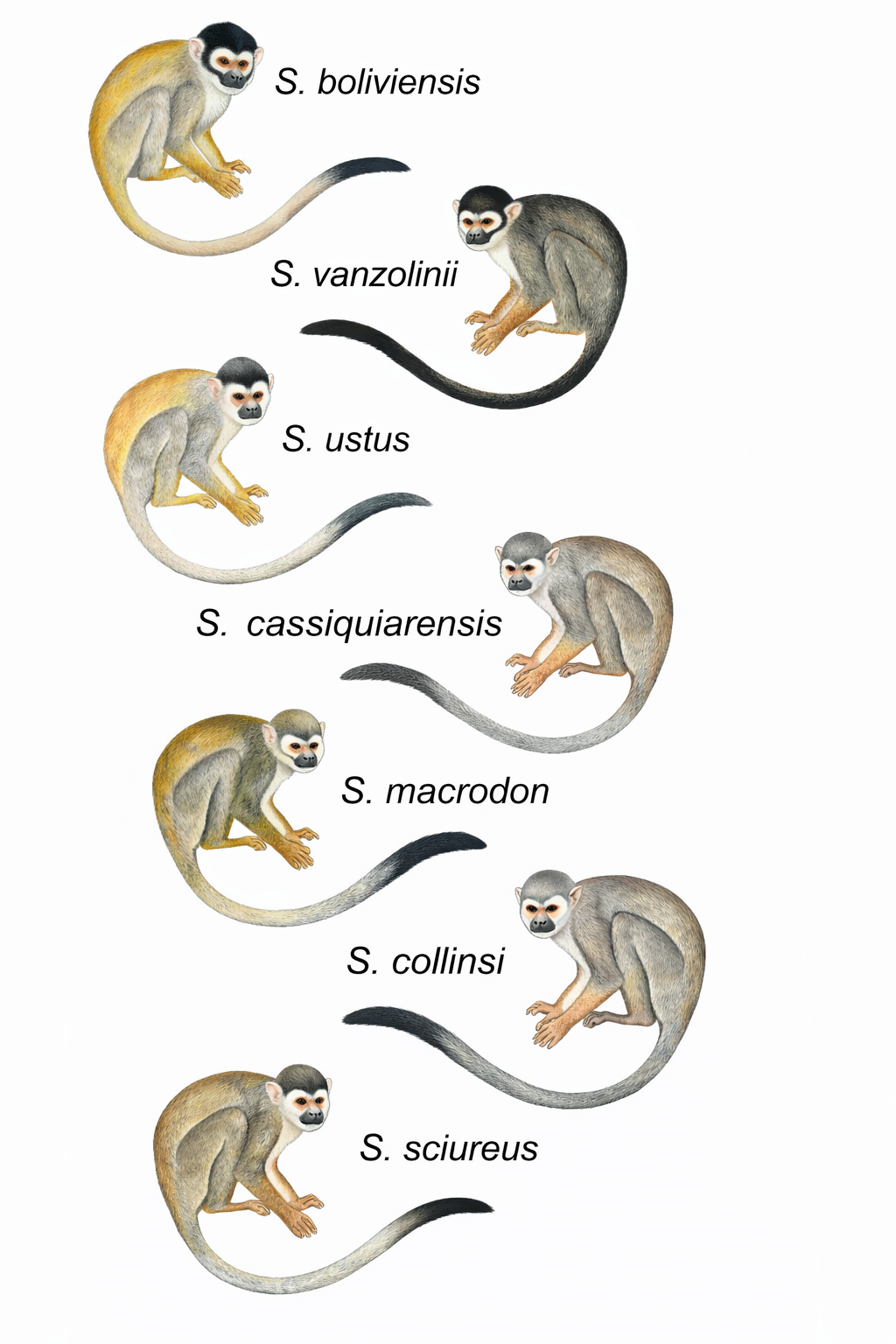 Todos los análisis filogenómicos (bayesianos, de máxima verosimilitud y de tiempos de divergencia) apoyaron de manera contundente la división de Saimiri en dos grandes clados, que coinciden perfectamente con los grupos morfológicos definidos por Hershkovitz: el grupo de arco gótico (Gothic) y el de arco romano (Roman). Dentro de ellos, se identificaron cinco linajes principales con un soporte máximo (probabilidad posterior de 1 y bootstrap de 100): (1) S. boliviensis + S. vanzolinii (grupo Romano); (2) S. ustus (el de orejas desnudas); (3) S. cassiquiarensis (noroeste amazónico); (4) S. macrodon (oeste amazónico); y (5) S. sciureus + S. collinsi (este amazónico). Esta topología resuelve las parafilias que mostraban los estudios mitocondriales previos y confirma la hipótesis morfológica, con la única excepción de una ligera parafilia en S. boliviensis que requerirá más muestreo.
Todos los análisis filogenómicos (bayesianos, de máxima verosimilitud y de tiempos de divergencia) apoyaron de manera contundente la división de Saimiri en dos grandes clados, que coinciden perfectamente con los grupos morfológicos definidos por Hershkovitz: el grupo de arco gótico (Gothic) y el de arco romano (Roman). Dentro de ellos, se identificaron cinco linajes principales con un soporte máximo (probabilidad posterior de 1 y bootstrap de 100): (1) S. boliviensis + S. vanzolinii (grupo Romano); (2) S. ustus (el de orejas desnudas); (3) S. cassiquiarensis (noroeste amazónico); (4) S. macrodon (oeste amazónico); y (5) S. sciureus + S. collinsi (este amazónico). Esta topología resuelve las parafilias que mostraban los estudios mitocondriales previos y confirma la hipótesis morfológica, con la única excepción de una ligera parafilia en S. boliviensis que requerirá más muestreo.